
Les vaccins pour le Covid-19 ont été distribués à une vitesse exceptionnelle et sans égal. Moderna aux États-Unis et BioNTech en Allemagne ont introduit un genre inédit de vaccin au public : celui basé sur l’ARNm, l’acide nucléique qui transmet habituellement les directives génétiques depuis le noyau de la cellule vers la zone de celle-ci où la fabrication de protéines se produit.

Les chercheurs ont mis au point divers médicaments et traitements pour dynamiser le système immunitaire des patients atteints de cancer
Comment a-t-on pu développer aussi vite cette technologie révolutionnaire ?
En réalité, cette méthode était en développement depuis une période prolongée, bien qu’elle n’ait pas été originellement conçue pour contrer les maladies virales. Son objectif principal résidait dans le traitement des cancers, déclare Özlem Türeci, co-fondatrice et médecin chef de BioNTech, l’entreprise ayant collaboré avec Pfizer pour la création du vaccin contre la Covid-19.
La rationalité derrière son application en oncologie se présente ainsi : étant donné que chaque tumeur est caractérisée par un ensemble de mutations génétiques qui n’apparaissent pas ailleurs dans l’organisme, il est théoriquement possible que notre système immunitaire identifie et élimine ces cellules. Malheureusement, les tumeurs ont la faculté d’inhiber le système immunitaire. En conséquence, les chercheurs ont mis au point divers médicaments et traitements pour dynamiser le système immunitaire des patients atteints de cancer.
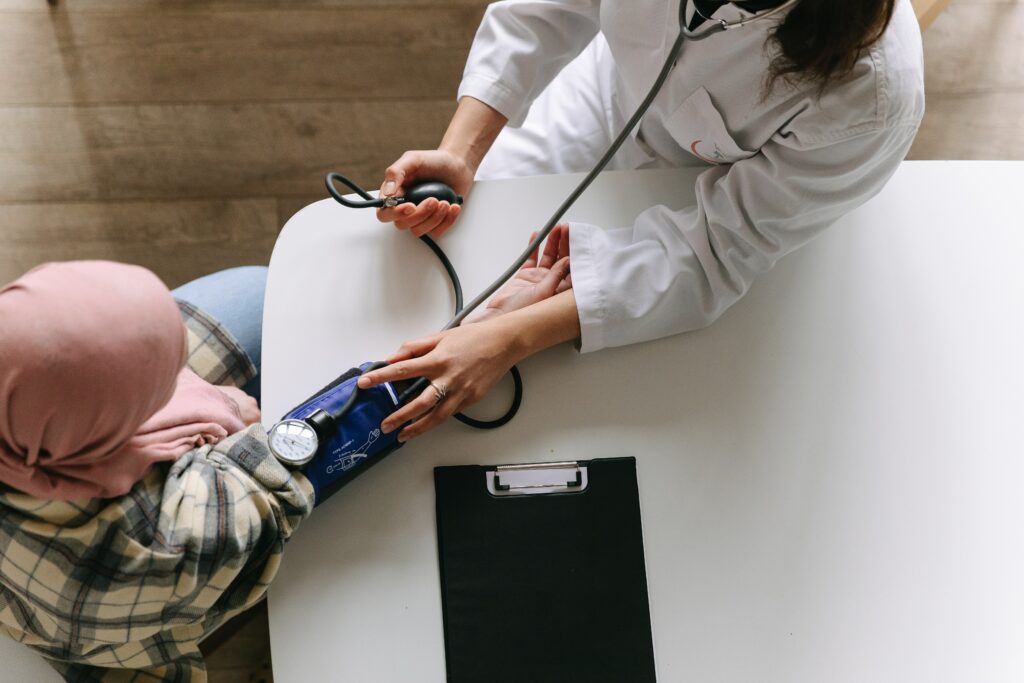
Il serait peut-être faisable d’introduire au système immunitaire du patient des fragments précis de tissu cancéreux afin de le préparer à attaquer la tumeur avec plus d’intensité
Cependant, un autre obstacle est que beaucoup de mutations tumorales parviennent à se faufiler sans être détectées. Face à cela, certains chercheurs ont suggéré une stratégie plus focalisée pour sensibiliser les cellules immunitaires aux mutations cancéreuses qu’elles ne visent pas naturellement, une approche qui s’apparente davantage à un vaccin. En effet, un vaccin fonctionne souvent en exposant les individus à un agent pathogène inactivé ou à certains de ses marqueurs spécifiques, préparant ainsi le système immunitaire à une réaction rapide en cas d’apparition de l’agent pathogène actif. Suivant cette logique, les scientifiques ont envisagé qu’il serait peut-être faisable d’introduire au système immunitaire du patient des fragments précis de tissu cancéreux afin de le préparer à attaquer la tumeur avec plus d’intensité. La configuration génétique d’une tumeur varie d’un individu à l’autre et continue d’évoluer au cours du temps.
L’un des bénéfices majeurs de l’emploi de l’ARNm dans cette tâche ne réside pas uniquement dans sa production relativement rapide, mais également dans sa grande adaptabilité
Ceci implique que l’idéal serait de personnaliser les vaccins et de les administrer à plusieurs reprises, ce qui est une démarche à la fois coûteuse et longue si l’on choisit de créer des fragments de protéines tumorales clés en laboratoire, une méthode qui était très répandue pour la fabrication des vaccins avant l’émergence de l’ARNm. Les protéines, élaborées à partir d’une diversité de vingt acides aminés, présentent des structures tridimensionnelles complexes et sont enclines à former des agrégats lorsqu’il y a une anomalie.
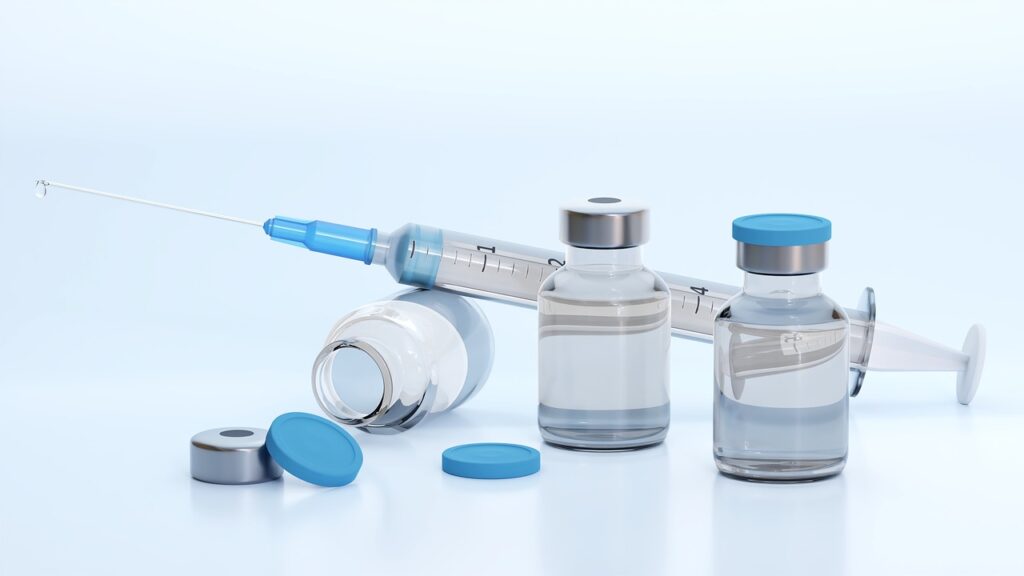
Une injection directe de vaccin à ARNm dans un ganglion lymphatique a déclenché une réaction immunitaire bien plus puissante que l’injection d’ARNm dans la peau ou le muscle, méthodes traditionnellement utilisées
Et si nous avions la capacité de produire des segments spécifiques d’ARNm, de les introduire dans l’organisme et de permettre aux cellules de synthétiser les protéines correspondantes elles-mêmes ? Ne serait-ce pas nettement plus simple ? Selon Türeci de BioNTech, leur technique consiste à injecter l’ARNm dans le corps où il est dirigé vers les ganglions lymphatiques. Ici, l’ARNm est traduit en protéines par un type de cellules immunitaires connu sous le nom de cellules dendritiques. Ces cellules présentent ensuite la protéine sur leurs surfaces, ce qui stimule les cellules T, qui surveillent nos tissus, pour identifier et éliminer les agents pathogènes portant la même marque.
La pandémie de Covid-19 a été un véritable test pour cette stratégie : en seulement une année, deux vaccins à ARNm extrêmement efficaces contre le virus SARS-CoV-2 ont été conçus, expérimentés et déployés. Il s’agit du vaccin Pfizer-BioNTech et du vaccin Moderna, chacun ayant une légère particularité. Les deux vaccins comportaient le code nécessaire pour produire une version stabilisée de la protéine spike que le virus utilise pour infiltrer les cellules. Le code de cette protéine spike a été intégré à l’ARNm avec une structure de support optimisée par des années de recherche. Cet ARNm a ensuite été enveloppé dans des lipides spécifiques pour garantir qu’il atteindrait bien ses ganglions cibles.
Türeci, co-auteur d’un article concernant les vaccins à ARNm contre le cancer publié dans l’Annual Review of Medicine en 2019, a discuté récemment avec le Knowable Magazine du progrès des vaccins à ARNm contre le cancer et du fait qu’ils sont sur le point d’être disponibles pour les patients ayant un besoin urgent de nouvelles thérapies.
L’interview a été éditée pour des considérations de longueur et de compréhension.
Quand a débuté le développement des vaccins contre le cancer et pourquoi pensait-on que l’ARNm serait plus efficace ?
Özlem Türeci : Il faut bien comprendre que tout ceci ne s’est pas réalisé du jour au lendemain. Il s’agit d’un périple s’étalant sur plusieurs décennies, ayant pris son essor dans les années 1990. À cette époque, notre ambition était vue comme relevant du domaine de la science-fiction : nous avions l’objectif de mettre au point des vaccins contre le cancer pour diminuer la taille des tumeurs. Le cancer de chaque patient est distinct car il découle de mutations aléatoires, c’est pourquoi nous nous sommes engagés à concevoir des vaccins personnalisés qui stimuleraient le système immunitaire du patient à combattre sa propre tumeur.
Nous avons expérimenté plusieurs méthodes, concluant que l’ARNm détenait le plus grand potentiel pour la création de vaccins anticancéreux véritablement personnalisés. L’ARNm synthétique, qui est le produit d’un processus simple et est très similaire à l’ARNm naturel, sert de modèle pour la protéine, ou l’antigène vaccinal, que les cellules de l’organisme sont capables de produire. Cependant, nous avons également compris que des améliorations importantes étaient nécessaires. Durant ces dernières décennies, nous avons travaillé à résoudre ces problèmes.
Nos recherches nous ont menés à la plateforme technologique basée sur l’ARNm que nous employons actuellement pour nos potentiels produits contre le cancer, les infections et d’autres maladies sévères. Parallèlement à nos travaux dans les années 1990, une poignée d’autres chercheurs s’est aussi intéressée à l’ARNm. Les progrès que nous avons tous réalisés ont servi de véritable catalyseur pour la communauté scientifique dans son ensemble.
Quels ont été les progrès clés qui ont facilité votre réussite jusqu’à présent ?
L’ARNm a longtemps souffert d’un défaut majeur : son efficacité réduite. Même en grandes quantités, l’ARNm générait une faible production de protéines, d’où un impact limité. C’est pour cette raison qu’à la fin des années 90, l’ARNm était peu considéré comme une nouvelle catégorie de médicaments dans le milieu médical. Les vaccins à ARNm expérimentés durant cette période ont généré de faibles réponses immunitaires.
Notre groupe de recherche a consacré de nombreuses années à l’analyse détaillée de chaque composant de l’ARNm. Nous avons trouvé plusieurs modifications susceptibles d’accroître sa stabilité et sa capacité à être traduit en protéine. Ainsi, nous avons élaboré des structures d’ARNm dont l’efficacité à provoquer des réponses immunitaires s’est avérée supérieure de plus d’un millier de fois.
Le prochain défi à résoudre consistait à déterminer comment acheminer le vaccin à ARNm aux cellules appropriées de l’organisme, ainsi qu’à identifier précisément ces cellules. En 2004, nous avons fait une découverte surprenante : une injection directe de vaccin à ARNm, en utilisant notre technique améliorée de colonne vertébrale, dans un ganglion lymphatique a déclenché une réaction immunitaire bien plus puissante que l’injection d’ARNm dans la peau ou le muscle, méthodes traditionnellement utilisées.
Quels sont les avantages majeurs de l’injection directe d’ARNm dans les ganglions lymphatiques pour une meilleure efficacité ?
Nous avons compris que l’acheminement des vaccins à ARNm vers les cellules dendritiques situées dans les ganglions lymphatiques s’avérait indispensable pour trouver une solution. Les années qui ont suivi ont été consacrées à la recherche de différentes techniques pour transporter l’ARNm vers ces zones précises du corps. Nous avons alors mis au jour que les vaccins à ARNm, enfermés dans une nanoparticule lipidique spécifique – une innovation que nous avons mise au point et que nous nommons lipoplexes à ARN –, étaient directement absorbés par les cellules dendritiques localisées dans les tissus lymphoïdes.
Ces cellules sont en quelque sorte les coachs d’élite du système immunitaire, capables de générer des réactions immunitaires particulièrement puissantes. Nous avons observé qu’elles possèdent un mécanisme particulier permettant d’ingérer des corps étrangers et de s’en servir pour entraîner le système immunitaire. Les réactions des lymphocytes T provoquées par le vaccin étaient exceptionnellement robustes, au point d’éliminer de larges tumeurs chez la souris. Ainsi, armés de ces découvertes et après avoir peaufiné notre technologie, nous sommes retournés auprès du patient.
Quelle est la séquence précise de votre transformation, de l’homme à la souris ?
En 2015, nous avons initié des recherches sur l’homme et élaboré la première livraison systémique de vaccins à nanoparticules d’ARNm chez l’homme. Dans certains cas, nous avons constaté une diminution de la taille des tumeurs chez nos patients souffrant de mélanome résistant aux traitements, grâce à l’utilisation du vaccin seul ou en combinaison avec des médicaments stimulant le système immunitaire. Ces résultats ont été documentés dans la revue Nature en 2017, jetant ainsi les bases pour le développement de vaccins à ARNm extrêmement efficaces.
Ces progrès nous ont rapprochés de notre objectif initial : l’élaboration de vaccins anticancéreux sur mesure adaptés à la tumeur du patient. Cette stratégie requiert l’analyse génomique de la tumeur d’un patient en utilisant le séquençage de nouvelle génération pour identifier les mutations spécifiques au cancer par rapport aux tissus sains du patient. Chaque patient présente un ensemble unique de mutations cancéreuses. Nous sélectionnons par la suite un certain nombre de ces mutations offrant la plus grande chance pour le système immunitaire de détecter le cancer, et nous concevons un vaccin sur mesure qui s’adapte à ce profil de mutations cancéreuses unique pour chaque patient.
Jusqu’à présent, combien de personnes ont bénéficié de vos vaccins à ARNm contre le cancer ?
Nous avons utilisé nos vaccins personnalisés en développement pour traiter plus de 450 patients. Ces vaccins sont spécialement conçus pour viser les mutations exclusives à chaque patient, propres à leur cancer spécifique. Par ailleurs, nous disposons d’un assortiment de vaccins anti-cancer à ARNm prêts à l’emploi. Ces vaccins comportent une association fixe d’antigènes tumoraux non mutés, encodés par l’ARNm, reconnus pour leur production fréquente dans certains types de cancer. Nous menons actuellement des recherches sur ces vaccins dans le cadre d’essais cliniques pour traiter divers cancers tels que le mélanome avancé, le cancer de la prostate et le cancer de la tête et du cou, avec plus de 250 patients traités à ce jour.
Tout ce travail est effectué dans le cadre d’essais cliniques. L’approche règlementaire du développement de ces traitements implique de traiter chaque type de cancer séparément et de façon indépendante pour chaque ligne de traitement concernée.
En termes de développement en oncologie, notre pipeline compte actuellement 20 programmes répartis sur 24 essais cliniques, dont cinq candidats en essais cliniques de phase avancée. En particulier, BNT111, un vaccin candidat à ARNm pour le traitement du mélanome avancé, a reçu la désignation accélérée de la FDA aux États-Unis. Cette désignation vise à faciliter et à accélérer le développement de nouveaux médicaments et vaccins destinés à traiter ou prévenir des maladies graves qui ont le potentiel de répondre à des besoins médicaux non satisfaits.
Pensez-vous que des modifications législatives seront nécessaires pour organiser l’approbation officielle des traitements spécifiques à chaque patient dans le cadre de la médecine personnalisée, où chaque patient reçoit un produit différent ?
Nous avons rapidement initié des dialogues avec les organismes de régulation. À notre avis, l’élément crucial est que la méthode de production et l’architecture de base de l’ARNm demeurent inchangées. Dans ce contexte, nous substituons simplement le code pour intégrer les mutations cancéreuses.
Le but d’un tel cadre serait que, indépendamment des mutations séquentielles utilisées pour personnaliser un vaccin, si tous les autres paramètres restent inchangés, il ne serait pas nécessaire de répéter un processus d’approbation complet pour une version personnalisée du vaccin. Cela à condition que le produit dans son ensemble ait déjà reçu l’approbation des autorités pour une certaine catégorie de tumeur. C’est ce vers quoi nous nous dirigeons, et je suis convaincu que nous y sommes presque. C’est également un domaine inexploré pour les organismes de régulation, un domaine où nous avons tous encore à apprendre.
Pourquoi a-t-il été si difficile de trouver un remède au cancer, et existe-t-il une raison fondamentale qui vous fait penser que les vaccins à ARNm pourraient offrir une solution là où d’autres approches ont échoué ?
L’une des raisons qui rend le cancer si redoutable, c’est sa complexité intrinsèque. Sa manifestation varie d’un individu à l’autre et évolue avec le temps. Toutefois, grâce à la polyvalence et la capacité de fabrication sur demande des vaccins à ARNm, nous avons la possibilité de les personnaliser. Nous sommes en mesure d’établir le profil mutationnel unique du cancer – son empreinte digitale si vous voulez – et de créer un vaccin spécialement adapté pour cibler ces mutations.
Si le cancer évolue chez un patient, provoquant une rechute, nous avons la capacité de modifier le traitement en conséquence. C’est une démarche similaire à celle que nous utilisons pour ajuster nos vaccins à ARNm Covid-19 face à l’émergence de nouvelles variantes virales inquiétantes.
Pourquoi le corps ne parvient-il pas à générer les bonnes cellules immunitaires en quantité suffisante pour éliminer une tumeur, nécessitant ainsi l’intervention d’un vaccin ?
D’abord, les tumeurs utilisent une variété de stratégies pour désactiver nos cellules immunitaires, non seulement dans l’ensemble du corps, mais aussi à l’intérieur de la tumeur elle-même. De plus, de nombreux aspects modifiés de la tumeur sont toujours perçus comme faisant partie intégrante de l’organisme, ce qui les rend tolérés par le système immunitaire. En conséquence, les cibles optimales pour le système immunitaire sont celles du mutanome tumoral : les mutations qui s’accumulent progressivement dans les cellules cancéreuses.
Cependant, seule une petite fraction de ces dernières est détectée par les cellules T circulantes spontanées. Avec nos vaccins candidats axés sur les mutations, nous cherchons à exploiter le potentiel du mutanome pour aider les cellules T à s’activer. Néanmoins, nous observons souvent qu’il faut un élément supplémentaire pour contrer la puissante inhibition immunitaire exercée par la tumeur. Cela pourrait être des modulateurs immunitaires comme les inhibiteurs des points de contrôle immunitaire ou la chimiothérapie, qui provoquent la mort des cellules cancéreuses et peuvent intensifier l’efficacité d’un vaccin.
Comment le développement de vaccins contre le cancer, avec sa pression temporelle due à la croissance continue des tumeurs non traitées, a-t-il contribué à votre réaction rapide face à la pandémie ? Quel est votre progrès actuel en matière de réduction du temps de développement du vaccin et quelles sont vos perspectives pour l’avenir en termes de délais d’administration aux patients ?
Le parcours qui débute par l’examen du génome de la tumeur d’un patient et se conclut avec la production sur mesure d’un vaccin à ARNm prêt à l’emploi, s’est avéré être une véritable lutte contre la croissance de la tumeur spécifique de ce patient. Depuis 2014, nous avons mis au point des vaccins personnalisés pour des centaines de patients atteints de cancer dans le contexte de nos essais cliniques et les avons distribués à travers le globe. Auparavant, ce processus prenait entre trois et cinq mois par patient. Actuellement, nous avons réduit ce temps à trois à six semaines, et j’anticipe que nous nous stabiliserons autour de trois semaines dans un futur proche.
Croyez-vous que les vaccins à ARNm contre le cancer pourront éventuellement bénéficier à tous ? Ou est-ce qu’il existe des tumeurs qui resteront toujours inaccessibles à ce type de traitement ?
Théoriquement, l’idée que les vaccins contre le cancer puissent être appliqués universellement est plausible, étant donné qu’à l’heure actuelle, aucune tumeur ne semble hors de portée de cette approche.
Cependant, il est important de tempérer cette perspective avec le fait que l’idée d’un vaccin contre le cancer qui éliminerait tous les problèmes relève plutôt d’une représentation idéalisée. Le cancer, en effet, est une maladie d’une complexité extrême.
Néanmoins, les vaccins contre le cancer pourraient devenir, dans le futur, une option stratégique qui enrichirait l’arsenal thérapeutique, apportant une contribution significative à l’amélioration du traitement des patients atteints de cancer.
SOURCE : Inverse
Traduit de l’anglais










