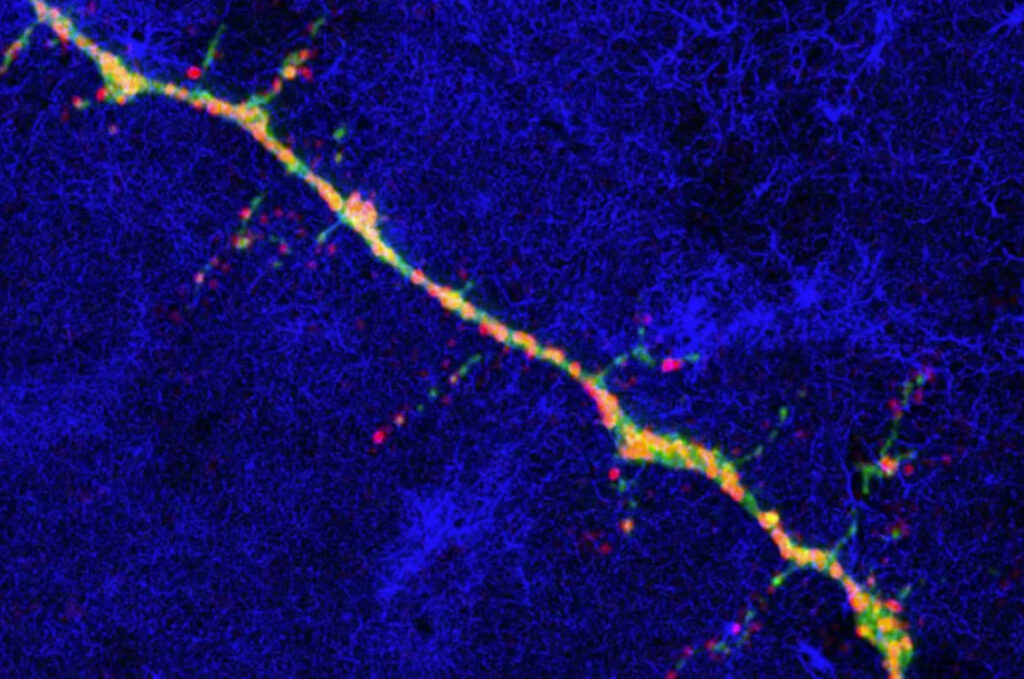
Les chercheurs ont utilisé des « molécules dansantes » pour faire avancer l’âge des neurones humains au-delà de ce qui était auparavant possible. Des chercheurs dirigés par l’Université Northwestern ont créé les premiers neurones hautement matures à partir de cellules souches pluripotentes induites par l’homme (CSPi), des progrès qui ouvrent de nouvelles opportunités pour la recherche médicale et les thérapies de transplantation potentielles pour les maladies neurodégénératives et les blessures traumatiques.
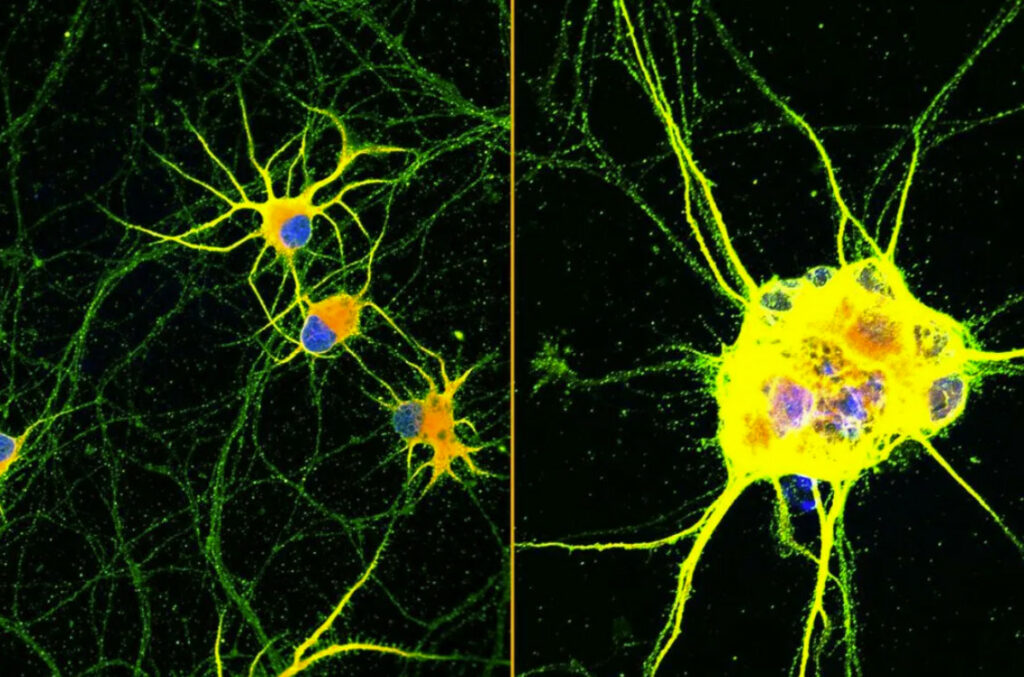
Images fluorescentes de neurones humains poussant sur des revêtements avec des molécules en mouvement rapide
Bien que des chercheurs précédents aient différencié les cellules souches pour devenir des neurones, ces neurones étaient fonctionnellement immatures, ressemblant à des neurones des stades embryonnaires ou postnataux précoces. La maturation limitée obtenue avec les techniques actuelles de culture de cellules souches diminue leur potentiel pour les études de neurodégénérescence, de sorte que les chercheurs de Northwestern ont décidé de danser sur un air différent, créant des neurones matures qui permettront la recherche de maladies d’apparition chez l’adulte dans des cultures cellulaires relativement simples et rentables.
Afin de créer des neurones matures, l’équipe de recherche a utilisé des « molécules dansantes », une technique révolutionnaire introduite fin 2021 par le professeur Samuel I.Stupp de Northwestern. L’équipe a d’abord différencié les CSPi humaines en neurones moteurs et corticaux, puis les a placés sur des revêtements de nanofibres synthétiques contenant les molécules dansantes se déplaçant rapidement.
Non seulement les neurones enrichis étaient plus matures avec des capacités de signalisation améliorées, mais ils ont également démontré une plus grande capacité de ramification, une qualité nécessaire pour que les neurones établissent un contact synaptique les uns avec les autres. De plus, contrairement aux neurones typiques dérivés de cellules souches qui ont tendance à s’agglutiner, ces neurones ne se sont pas agrégés, ce qui les rend moins difficiles à maintenir.
Écrivant dans Cell Stem Cell, les chercheurs pensent qu’avec un développement ultérieur, ces neurones matures pourraient être transplantés chez des patients comme une thérapie prometteuse pour les lésions de la moelle épinière ainsi que les maladies neurodégénératives, y compris la sclérose latérale amyotrophique (SLA), la maladie de Parkinson, la maladie d’Alzheimer ou la sclérose en plaques.
Afin de créer des neurones matures, l’équipe de recherche a utilisé des « molécules dansantes », une technique révolutionnaire introduite fin 2021 par le professeur Samuel I Stupp de Northwestern
Les neurones matures présentent également de nouvelles opportunités pour l’étude des maladies neurodégénératives comme la SLA et d’autres maladies liées à l’âge dans des modèles in vitro basés sur des boîtes de culture. En avançant l’âge des neurones dans les cultures cellulaires, les chercheurs pourraient améliorer les expériences pour mieux comprendre les maladies tardives.
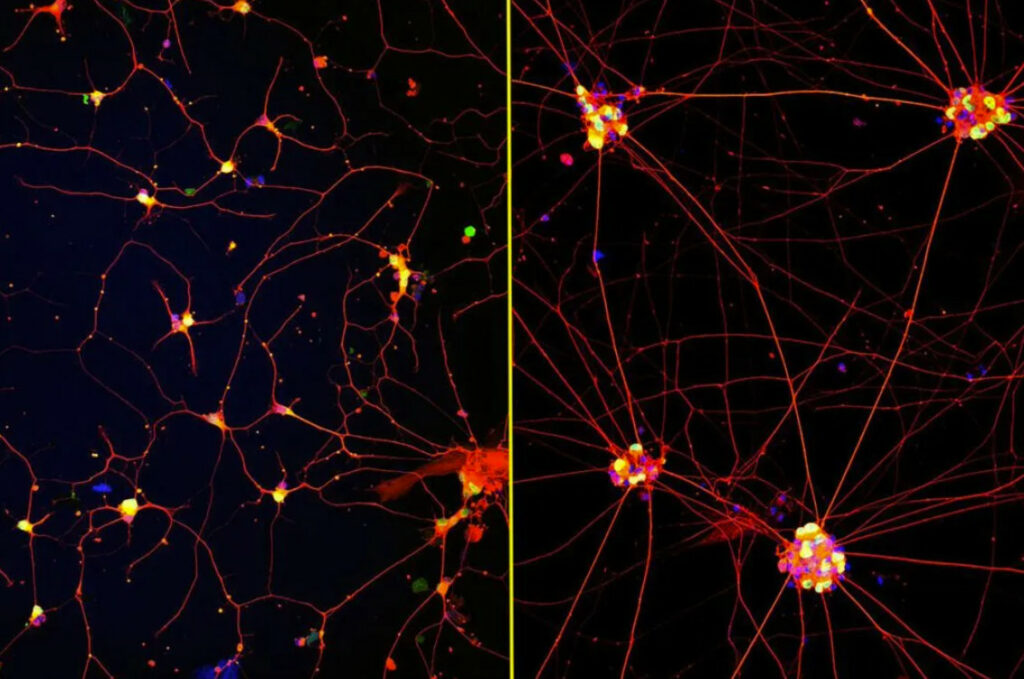
Images fluorescentes de neurones humains (colorés en rouge, vert et bleu) poussant sur des revêtements avec des molécules en mouvement rapide (à gauche) ou de la laminine conventionnelle (à droite) pendant 72 heures
« C’est la première fois que nous avons pu déclencher une maturation fonctionnelle avancée de neurones humains dérivés de l’iPSC en les plaquant sur une matrice synthétique », a déclaré Evangelos Kiskinis de Northwestern, co-auteur correspondant de l’étude.
« C’est important parce qu’il existe de nombreuses applications qui obligent les chercheurs à utiliser des populations purifiées de neurones. La plupart des laboratoires à base de cellules souches utilisent des neurones de souris ou de rats co-cultivés avec des neurones dérivés de cellules souches humaines. Mais cela ne permet pas aux scientifiques d’étudier ce qui se passe dans les neurones humains parce que vous finissez par travailler avec un mélange de cellules de souris et humaines. »
« Lorsque vous avez un iPSC que vous parvenez à transformer en neurone, ce sera un jeune neurone », a déclaré Stupp, co-auteur correspondant de l’étude. Mais, pour qu’il soit utile dans un sens thérapeutique, vous avez besoin d’un neurone mature. Sinon, c’est comme demander à un bébé d’effectuer une fonction qui nécessite un être humain adulte. Nous avons confirmé que les neurones recouverts de nos nanofibres atteignent plus de maturité que d’autres méthodes, et les neurones matures sont mieux en mesure d’établir les connexions synaptiques qui sont fondamentales pour la fonction neuronale.
Capacités de « danse » synchronisées
Pour développer les neurones matures, les chercheurs ont utilisé des nanofibres composées de « molécules dansantes », un matériau que le laboratoire de Stupp a développé comme traitement potentiel des lésions aiguës de la moelle épinière. Dans des recherches antérieures, Stupp a découvert comment régler le mouvement des molécules, afin qu’elles puissent trouver et interagir correctement avec les récepteurs cellulaires en mouvement constant ; en imitant le mouvement des molécules biologiques, les matériaux synthétiques peuvent communiquer avec les cellules.
Une innovation clé de la recherche de Stupp a été de découvrir comment contrôler le mouvement collectif de plus de 100 000 molécules dans les nanofibres. Parce que les récepteurs cellulaires dans le corps humain peuvent se déplacer à des vitesses rapides, parfois à des échelles de temps de quelques millisecondes, ils deviennent des cibles mobiles difficiles à atteindre. « Imaginez diviser une seconde en 1 000 périodes », a déclaré Stupp. « C’est ainsi que les récepteurs pourraient se déplacer rapidement. Ces délais sont si rapides qu’ils sont difficiles à saisir. »
Dans la nouvelle étude, Stupp et Kiskinis ont découvert que les nanofibres réglées pour contenir les molécules avec le plus de mouvement conduisaient aux neurones les plus améliorés. En d’autres termes, les neurones cultivés sur des revêtements plus dynamiques, essentiellement des échafaudages composés de nombreuses nanofibres, étaient aussi les neurones qui devenaient les plus matures, les moins susceptibles de s’agréger et avaient des capacités de signalisation plus intenses.
« La raison pour laquelle nous pensons que cela fonctionne est que les récepteurs se déplacent très rapidement sur la membrane cellulaire et que les molécules de signalisation de nos échafaudages se déplacent également très rapidement », a déclaré Stupp. Ils sont plus susceptibles d’être synchronisés. Si deux danseurs ne sont pas synchronisés, le jumelage ne fonctionne pas. Les récepteurs sont activés par les signaux lors de rencontres spatiales très spécifiques. Il est également possible que nos molécules en mouvement rapide améliorent le mouvement des récepteurs, ce qui contribue à leur regroupement pour bénéficier de la signalisation.
Les neurones avec la signature de la SLA offrent une nouvelle fenêtre sur la maladie
Stupp et Kiskinis croient que leurs neurones matures donneront un aperçu des maladies liées au vieillissement et deviendront de meilleurs candidats pour tester diverses thérapies médicamenteuses dans des cultures cellulaires. En utilisant les molécules dansantes, les chercheurs ont pu faire progresser les neurones humains à des âges beaucoup plus avancés qu’auparavant, permettant aux scientifiques d’étudier l’apparition de maladies neurodégénératives.
Dans le cadre de la recherche, Kiskinis et son équipe ont prélevé des cellules cutanées d’un patient atteint de SLA et les ont converties en CSPi spécifiques au patient. Ensuite, ils ont différencié ces cellules souches en motoneurones, qui est le type de cellule atteint dans cette maladie neurodégénérative. Enfin, les chercheurs ont cultivé des neurones sur les nouveaux matériaux de revêtement synthétiques pour développer davantage les signatures de la SLA. Non seulement cela a donné à Kiskinis une nouvelle fenêtre sur la SLA, mais ces « neurones de la SLA » pourraient également être utilisés pour tester des thérapies potentielles.
« Pour la première fois, nous avons pu observer l’agrégation des protéines neurologiques à l’âge adulte dans les motoneurones des patients atteints de SLA dérivés de cellules souches. Cela représente une percée pour nous », a déclaré Kiskinis. « On ne sait pas comment l’agrégation déclenche la maladie. C’est ce que nous espérons découvrir pour la première fois. »
Espoirs pour le traitement futur des lésions de la moelle épinière et des maladies neurodégénératives
Plus tard, des neurones matures et améliorés dérivés de l’iPSC pourraient également être transplantés chez des patients atteints de lésions de la moelle épinière ou de maladies neurodégénératives. Par exemple, les médecins pourraient prélever des cellules cutanées d’un patient atteint de SLA ou de la maladie de Parkinson, les convertir en CSPi, puis cultiver ces cellules sur le revêtement pour créer des neurones sains et hautement fonctionnels.
La transplantation de neurones sains chez un patient pourrait remplacer les neurones endommagés ou perdus, restaurant potentiellement la cognition ou les sensations perdues. Et, parce que les cellules initiales provenaient du patient, les nouveaux neurones dérivés de l’iPSC correspondraient génétiquement au patient, éliminant ainsi la possibilité de rejet.
« La thérapie de remplacement cellulaire peut être très difficile pour une maladie comme la SLA, car les motoneurones transplantés dans la moelle épinière devront projeter leurs longs axones vers les sites musculaires appropriés à la périphérie, mais pourraient être plus simples pour la maladie de Parkinson », a déclaré Kiskinis. « Quoi qu’il en soit, cette technologie sera transformatrice. »
« Il est possible de prendre des cellules d’un patient, de les transformer en cellules souches, puis de les différencier en différents types de cellules », a déclaré Stupp. « Mais le rendement de ces cellules a tendance à être faible, et atteindre une bonne maturation est un gros problème. Nous pourrions intégrer notre revêtement dans la fabrication à grande échelle de neurones dérivés de patients pour des thérapies de transplantation cellulaire sans rejet immunitaire. »
SOURCE : Longevity.Technology
Traduit de l’anglais